Bir Vakum Yaratmaya Neden İhtiyaç Duyariz?
Bi̇r Vakum Yaratmaya Neden İhti̇yaç Duyariz?
Bir vakum yaratmak oldukça yaygın ve çoğu zaman rutin bir girişim haline gelmiştir. Ancak faaliyetin yaygın olması onun maliyeti ve zorluklarını maskelememektedir. İnsanlar vakum teknolojisi ile çok iyi bir nedenden dolayı mücadele etmektedir. Vakumlar bir dereceye kadar süreçleri yürütmenin zorunlu bir parçasını teşkil eder ve/veya bir ürünün entegre bir parçasıdır.

Her bir vakum uygulayıcısına, şu yada bu zamanda, neden son mermer taşlarını kaybetmeyi riske atma noktasına kadar gidecek şekilde tüm bu deneme, çalışma ve sıkıntılara katlanmaya gerek duydukları sorulmuştur. Geçici olarak kabul edilebilir yanıtlardan biri “Bunu yapmalıyım, yaptığım her ne ise onu yapmalıyım” dır. Bununla birlikte çok gerçek ve basit yanıtlar mevcuttur. Temel olarak her ne yapılacak ise onu yapmak için bir kaptan (hazne) belirli sayıdaki molekülü ortadan kaldırmak zorunludur. Bunun ardından konuyu biraz daha ayrıntılandırırsanız soru o kadar da ürkütücü değildir.
Bir vakum yaratmanın bir kaptaki gaz moleküllerini hacim başına düşen molekül sayısı kap dışındaki hacim başına düşen molekül sayısından daha düşük olana kadar ortadan kaldırmaktan başka bir şey olmadığını dikkate alır isek bunu yapmak için bir dizi sebepler geliştirmeye başlayabiliriz. .
Bu azaltılmış molekül popülasyonu, basınç, molekül sayısı, moleküller arasındaki mesafe, molekül çarpışmalarının sayısı yada moleküllerin bir yüzey ile çarpışma sayısı olarak görülebilir. Tüm bu görünümler fiziksel olarak birbirleri ile bağlantılı ve karşılıklı olarak birbirine bağlı olsa bile, bu olası sebeplerin herhangi biri ilgili gereklilikler ve doğrulamalar ile bir süreç tanımı içine götürülebilir.
Her iki fiziksel ve kimyasal etkiler ya ayrı olarak yada birleşik olarak devreye girer.
Fi̇zi̇ksel Etki̇ler
Fiziksel etkiler gaz yada gazların fiziksel etkilerinin ya sürecin ana odak noktası olacağı yada sürece yardımcı olacağı yada süreci engelleyeceği durumlarda devreye girer.
Basinç Di̇feransi̇yeli̇Bir boru yada kaptan gaz molekülleri ortadan kaldırıldığı zaman moleküller arasında daha az etkiler olacak ve bunun ardından kabın atmosfer etkisine açık olduğu dış tarafı üzerinde bir yüzey meydana gelecektir. Moleküllerin sayısı ne kadar az olursa çarpışmaların sayısı da o kadar az olur ve dolayısıyla da sonuçta ortaya çıkacak toplam kuvvet de daha düşük olacaktır.
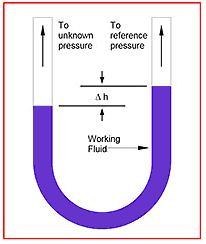
Şekil 1 –U-tüp manometresi
Birçok fiziksel etkilerde olduğu gibi bu da basınç ile orantılı bir kuvvet tatbik etmek suretiyle basınç diferansiyelini kullanarak basıncı ölçmek için kullanılabilir. Bu husus, bir sıvı sütunun, Şekil 1’de gösterildiği gibi ölçülebilir bir sıvı sütun ile sonuçlanacak bir şekilde diferansiyel basınca reaksiyon göstermek suretiyle atmosfer basıncına karşı dengelendiği U-tübü manometre tarafından kolayca gösterilir.
Pratik bir süreç anlamında, molekülleri bir yüzey ile çarpışan moleküllerin sayısını azaltacak bir şekilde ortadan kaldırmanın bir sonucu olarak ortaya çıkan bu basınç diferansiyeli hem dinamik hem de statik modlarda güç sağlamak için kullanılabilir.
Dinamik uygulamalar çoğu zaman katı yada sıvı maddeleri yüksek atmosfer basıncının malzemeyi her iki taraftaki basıncı eşitleştirmek amacıyla düşük basınca doğru sürüklediği bir boru içinden hareket ettirmek için kullanılır. Pnömatik aktarma tübü, vakum ile aktive olan filtreleme yada ilk metro gibi harekete geçirme kuvvetinin gerekli olduğu örnekler boldur. Statik bir anlamda basınç diferansiyeli çoğu zaman vakum savrulması yada tutmacı gibi durumları yerli yerine oturtmak imkanı sağlamak için kullanılır. Şekil 2’de psi’deki basınç diferansiyelini basınç ile değişkenlik gösterdiği süreçte göstermektedir.
ISI TRANSFERİ
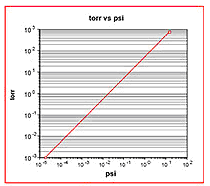
ŞEKİL 2: Psi vb.’de tor cinsinden basınç diferansiyeli
Atmosfer basıncında ısı transferi ağırlıklı olarak ya gaz molekülü – molekül çarpışmaları sırasında doğrudan aktarma tarafından yada moleküler hareket konveksiyonu tarafından yerine getirilir. Farklı ısılara sahip olan iki obje atmosfer basıncı altında bir hazneye yerleştirilirse, ısı, gaz molekülleri içinden geçerek daha sıcak olandan daha soğuk olana doğru akmaya başlayacaktır; ancak gaz moleküllerinden bazılarını ortadan kaldırmak suretiyle basınç azaltılırsa moleküller arasındaki mesafe daha uzun olacak ve moleküler çarpışmaların sayısı daha az olacak ve bunun sonucu olarak da ısı akışı azalacaktır.
Isı transferi ortamının (gaz molekülleri) termal iletkenliğinin azalması daha sıcak objelerin ısısını muhafaza etme eğiliminde olacağı anlamına gelir. Basınç sürekli olarak azalırsa ısı akışı da sürekli olarak azalacaktır.
Dolayısıyla sıcak ve soğuk objeler arasındaki vakum bir termal yalıtkan haline gelecek ve yalıtım derecesi bu objeler arasındaki vakum derecesi ( moleküllerin kıtlığı) tarafından belirlenecektir.Vakumun bu yalıtıcı etkisi bir dizi pratik uygulamalara yol açar.
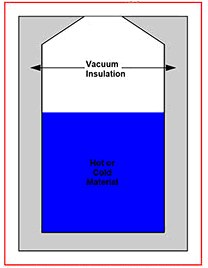
Şekil 3: Dewar termosunun şematik görünüşü
Bunun belki de en iyi örneği şekil 3’de gösterilen ve nesneleri sıcak yada soğuk tutmak amacıyla yaygın olarak kullanılan eski dewar termosu yada termos şişesidir. Bu, kolayca, ısının sıvıya ulaşıp buharlaşmasına neden olmasını engellemek için tüpler arasında bir vakum ile donatılmış bir halkalı tüp ile çevrelenmiş olan sıvılaşmış gazlar için aktarma hatları gibi diğer uygulamalara yol açar.
Basınç diferansiyellerinden kaynaklanan mekanik etkilerde olduğu gibi, termal iletkenlik bir basınç ölçme tekniği olarak kullanılabilir. Bu bağlamda bir kablo sabit bir güç uygulamak suretiyle ısıtılır ve kablonun ısı kaybı ya doğrudan ölçülen (ısı ölçeri) yada radar direnci tarafından ölçülen (pirani vakum ölçeri) ısısı tarafından gösterilir.
Isı iletkenliğinde bulunan etkiler ile aynı etkiler bazı spesifik kompleks farklılıklar ile birlikte ses yada elektrik yalıtım için de uygulanabilir.
Buharlaşma
Her türlü madde yeterince ısıtıldığı takdirde esas itibariyle buharlaşacaktır ancak vakum süreçleri en çok akıcı maddelerin buharlaşması ile ilgili olma eğilimindedir. Oda ısısında herhangi bir uçuculuğa sahip olmayan bir sıvı atmosfer basıncında er yada geç buharlaşacaktır. Bir pratik süreç açısından sürecin daha erken meydana gelmesi daha geç meydana gelmesinden genel olarak daha iyi olacaktır ve dolayısıyla buharlaşma oranını arttırma araçları önemli olabilir.
Buharlaşmanın gerçekte yüzeyden ayrılan ve sıvı olarak geri dönmeyen sıvı molekülleri olması nedeniyle buharlaşma hızının arttırılması verili bir zamanda ayrılan moleküllerin sayısını arttırma anlamına gelecektir.
Atmosfer basıncında kayıp oranı doğrudan yüzeyin üzerindeki moleküllerin sayısının yüksek olması nedeniyle kayıp hızı göreceli olarak yavaş olacaktır. Bu , buharlaşan bir molekülün muhtemelen derhal bir gaz molekülüne çarpacağı , enerjisini kaybedeceği ve sıvı hale geri döneceği anlamına gelir. Ancak bir hazne içindeki sıvı bir ölçüye kadar boşaltılmış ise yüzeyin üzerinde daha az sayıda molekül olacaktır. Bu, vuracak molekül sayısının daha az olması, moleküller arasında daha büyük alanlar olması ve sıvı yüzeye çarpan molekül sayısının daha az olması nedeniyle buharlaşan bir molekülün bir gaz molekülüne çarpma şansının daha az olacağı anlamına gelir.
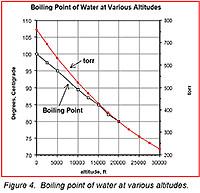
Şekil 4: Farklı rakımlarda suyun kaynama noktası
Bunun pratik bir örneği suyun kaynama noktasının vadi ve dağ zirvesi arasında gösterdiği farklılıktır. Bir sıvı kaynadığı zaman, sıvıya ilave olunan ısının hemen buharlaşmaya dönüştüğü ve dolayısıyla sıvının ısısının değişmeyeceği kritik bir noktaya ulaşmış demektir. Rakım yükseldikçe basınç azalır ve dolayısıyla buharlaşmayı engelleyen daha az sayıda molekül vardır ve buharlaşan moleküllerin ortamdaki gaz moleküllerinden gelen çarpışma kaynaklı kayıpların üstesinden gelmesi için daha az enerji gerekir. Şekil 4’de suyun farklı rakımlardaki kaynama noktasındaki farklılıklar gösterilmektedir.
Pratik bir vakum süreci farklı buhar basınçlarına sahip olan iki sıvıyı ayırmanın gerekli olduğu vakum damıtmadır. Sıvı karışımının bir tabakasının sabit bir ısıda boşaltılmış bir kap içine akması en uçucu bir sıvıyı bile düşük bir ısıda buharlaşmaya zorlayacak yada düşük bir ısıda buharlaşmasına olanak sağlayacaktır çünkü buharlaşmayı engellemek için atmosfer basıncında mevcut olandan daha az sayıda molekül mevcut olacaktır.
Dolayısıyla bu pratik bir süreç için birinci damıtmadır. Düşürülmüş bir basıncı sürdürmek için kabın dinamik olarak pompalanmasının gerektiği anlaşılmalıdır , aksi takdirde kaçan moleküller, kısa bir süre sonra, basıncın artmasına neden olacak ve sonra da sıvının buharlaşma hızını düşürecektir. Bu tür bir sürecin örneği mekanik pompa yağının bir vakumlu pompada kullanılabilmesinden önce yüksek buhar basınçlı uçucu bileşenlerinin ortadan kaldırılmasının gerekli olduğu mekanik pompa yağının damıtılması işlemidir.
Kimyasal Etkiler
Kimyasal etkiler, gazların kimyasal reaktivitesi ve özelliklerinin bir sürece ya yardım edeceği yada o süreci engelleyeceği birçok durumda devreye girer. Bu olgu yalnızca söz konusu muayyen gazlar değil aynı zamanda onların ilgili konsantrasyonları ile de ilgilidir.
Reakti̇f Gazlarin Ortadan Kaldirilmasi
Herhangi bir kap, hazne yada tesisat kullanım ömrü boyunca herhangi bir zamanda atmosfer havasının etkisine maruz kalır. Bu sayılan objelerden herhangi birinin saf proses gazını kontrol altına almak yada aktarmak için kullanılmasından önce, saf gaz devreye sokulmadan önce içerideki gazların zararlı etkilerini en aza indirgemek için tahliye edilmeleri gerekir. Eğer bu işlem yapılmaz ise bu durum saflaştırılmış bir kimyasal çözeltiyi kirli bir deney şişesi içine dökmeye çok benzeyecektir. Gerekli gazın saflık derecesi gerekli olan nihai vakumu belirleyecektir çünkü artık gazların popülasyonunun tümü kirletici madde olarak addedilecektir.
Örneğin 10(-3) tor’luk bir oksijen basıncı, kap saf gaz ile atmosfer basıncına geri doldurulmuş ise 1 PPM’lik bir kirlilik seviyesi ile sonuçlanacaktır. Bu basit artık gaz basıncı konsepti yanıltıcı olabilir çünkü iç yüzeyler yüzey bir kere saf gaz ile denkleştirildiği zaman kirlilik seviyesini PPM’nin onlarca katına kadar çıkaracak olan ayrışan su molekülleri ile kaplanacaktı. Dolayısıyla kap içindeki moleküllerin toplam sayısı bu tip bir etki söz konusu olduğunda başlıca ilgi noktası olacaktır.
Bu etkiyi göstermek için pratik bir uygulama atıl gaz ile geri dolgu işlemi yapmadan önce boşaltılacak olan eski göz kamaştırıcı elektrik ampulüdür. Geri dolgu işleminden önce ampulün gövdesinde kalan herhangi bir su buharı yada oksijen operasyon sırasında sıcak tungsten filamenti ile reaksiyona girecek olan kimyasal olarak aktif bir kirletici madde haline gelir ve zamanından önce yanıp tükenmeye neden olur.
Koruma
Birçok maddeler hava ile kimyasal reaksiyon içine girdiği için işleme tabi tutulan yüzeyin civarından molekülleri ortadan kaldırmak gerekli hale gelir. Bunu yapmanın yegane makul yolu malzemeleri bir hazne içine yerleştirmek ve malzemeleri bir kimyasal reaksiyondan korumak için atmosferi yada atmosferin yokluğunu kullanmaktır. Bu durumda yüzeye çarpan kimyasal olarak reaktif gazın moleküllerinin sayısı birincil bir öneme sahip olacaktır.
Bazı süreçlerde hazne yukarıda tartışılan bağlantılar ile aynı bağlantıları kullanarak tahliye edilecektir. Şöyle ki, hazne, sürecin dayattığı kadar çok sayıda reaktif gaz moleküllerini imha etmek için tahliye işleminin ardından atıl gaz ile geri doldurulacaktır. Diğerlerinde tüm süreç, materyali kimyasal reaksiyondan korumak için vakum altında gerçekleşir.
Metalürjik süreçler bir fırının boşaltılabileceği ve sonra da atıl gaz yada hidrojen (atmosferi azaltan) ile geri doldurulabileceği yada hazne dinamik pompalama şartları altında iken tüm ısıl sürecin yürütülebileceği başlıca örneklerdir Gerçekte vakum lehimleme gibi süreçler çoğu zaman fırının, başlangıçtaki tahliye işleminin ardından, bir hidrojen basıncı ile doldurulmuş iken ön ısıtmadan geçirildiği ve haznenin lehimleme ısısına ulaşmadan hemen önce boşaltıldığı ve sonra da lehimleme alaşımı akış ısısına ani bir yükselme verildiği kombine süreçlerdir.
Birleşik Fiziksel ve Kimyasal Etkiler
İnce tabaka süreçleri fiziksel ve kimyasal etkilerin bir kombinasyonunu gerektiren süreçlerin başlıca örnekleridir. Alüminyumun Şekil 5’de gösterildiği gibi bir alt katman üzerine telciksi olarak buharlaşması şeklindeki basit örneği düşünün. Bükülü bir tungsten filament bir alüminyum zımba teli eriyene ve filamenti ıslatana kadar doğrudan yüksek akım tarafından ısıtılır. Kimyasal olarak aktif gazların moleküler konsantrasyonu çok yüksek ise filament oksitlenecek ve yanıp tükenecektir. Buna ilaveten sıcak alüminyum oksitlenecektir. Bu durumda aktif gazların yüzeye çarpış sayısı büyük bir öneme sahiptir. Isıtma işlemi bir atıl gaz atmosferi altında yapılabilecek olsa bile bu, süreç parametresi gerekliliklerinin komple setinin yalnızca bir parçasıdır. Amaç alüminyum moleküllerini alt katman üzerine buharlaştırmak olduğuna göre buharlaşan alüminyum için alt katmana ulaşmak mümkün olmalıdır.
Buharlaşan alüminyum ve alt katman arasındaki molekül sayısı çok yüksek olsa idi alüminyumdan gaza molekül çarpışmaları o kadar yüksek olacaktı ki alüminyum çarpışmalardan doğan enerji kaybına bağlı olarak muhtemelen alt katmana ulaşmaya muktedir olmayacaktı. Buna ilaveten hafifçe daha düşük bir gaz molekülü konsantrasyonu buharlaşan alüminyum konsantrasyonunda yeterli bir dağılmaya kolayca neden olabilir ve bunun sonucu olarak alt katman üzerindeki tabaka kabul edilebilir bir eşbiçimlilikten yoksun olacaktır.
Sonuçlar
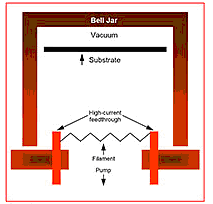
ŞEKIL 5: ALÜMINYUMUN BASIT FILAMANTER BUHARLAŞMASI SISTEMI
Şu halde artık tüm vakum süreçlerinin molekül sayısı ve elbette o moleküllerin kimyasal faaliyet açısından kimliği açısından özel gerekliliklere sahip oldukları açıktır. Bu moleküler etkilerin, basınçları, molekül sayısı, moleküller arasındaki mesafe, moleküler çarpışmaların sayısı yada moleküllerin bir yüzey ile çarpışma sayısı açısından nedenlerinin anlaşılması inceleme konusu olan sürecin daha iyi anlaşılmasını sağlayabilir Etkiler hakkında biraz daha düşünülmesi, iyileştirmeler birbiri ile aynı metotları akılda tutarak öngörüldüğü için daha iyi bir süreç elde edilmesine yol açabilir.
Moleküllerin incelemesi üzerinde daha da durmak sürecin o şekilde kavranmasını iletmenin daha iyi yollarını açabilir.
